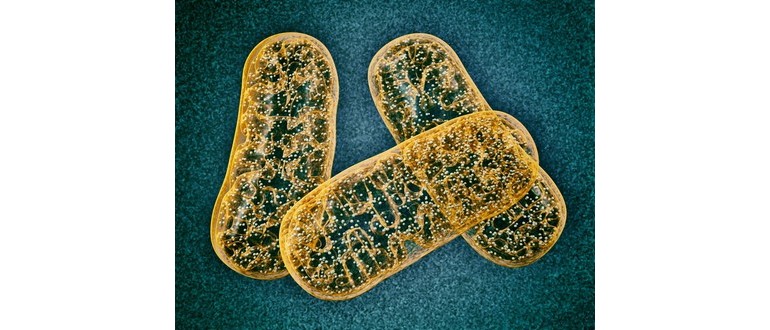
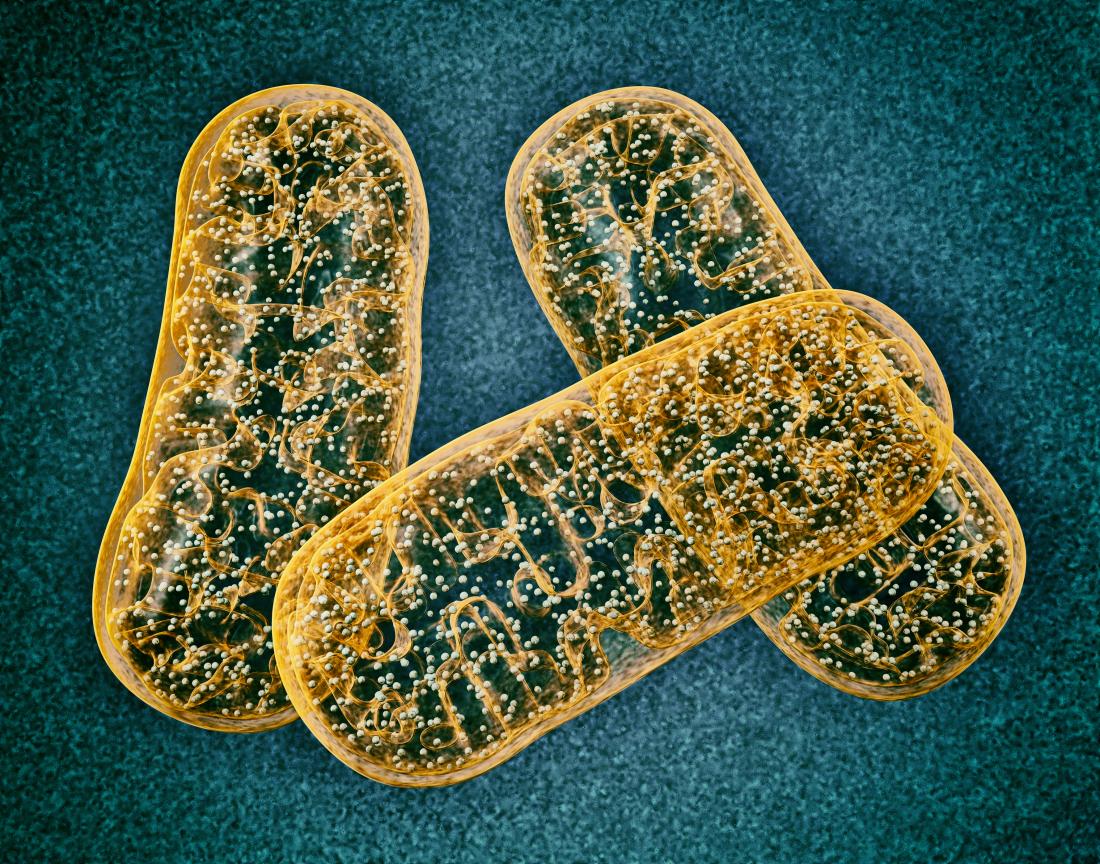
Lesioni ai mitocondri – piccole centrali elettriche all’interno delle cellule che forniscono loro energia – innescano eventi che si verificano presto nella malattia di Alzheimer e possono offrire un obiettivo promettente per il trattamento.
Così conclude un nuovo studio pubblicato sulla rivista che mostra come la beta amiloide oligomerica – una proteina altamente tossica – sconvolga i mitocondri.
Lo studio rivela anche come un pretrattamento possa proteggere le cellule cerebrali umane da tali danni.
«I mitocondri», afferma l’autore principale Dr. Diego Mastroeni, un assistente professore presso l’Arizona State University di Tempe, «sono la principale fonte di energia nelle cellule cerebrali e le carenze nel metabolismo energetico hanno dimostrato di essere uno dei primi eventi nella malattia di Alzheimer patobiologia.»
L’Alzheimer è una malattia devastante che distrugge il tessuto cerebrale e deruba le persone della loro capacità di pensare, ricordare, prendere decisioni, socializzare e vivere in modo indipendente.
È la forma più comune di demenza e la sesta causa principale di morte negli Stati Uniti, dove più di 5 milioni di persone hanno la condizione.
Il peso della malattia di Alzheimer negli Stati Uniti sta crescendo con l’invecchiamento della popolazione. Il costo di Alzheimer e altre forme di demenza aumenterà da $ 259 miliardi a $ 1,1 trilioni tra il 2017 e il 2050.
Man mano che progredisce, la malattia cambia la biologia e la chimica del cervello, causando la scomparsa delle cellule nervose o dei neuroni e il restringimento dei tessuti.
Non esiste attualmente alcuna cura o trattamento efficace che rallenti in modo significativo il progresso della malattia di Alzheimer.
Si sa che i segni del primo cambio di tessuto sono in corso prima che emergano i sintomi comportamentali dell’Alzheimer; tuttavia, nonostante alcune forti teorie, le cause esatte rimangono un mistero.
Beta amiloide e malattia di Alzheimer
Una teoria dominante sulle origini dell’Alzheimer propone che l’accumulo di frammenti proteici appiccicosi chiamato beta amiloide inneschi la catena di eventi nel cervello che porta alla malattia.
L’evidenza principale a sostegno di questa teoria dell’amiloide è che le autopsie cerebrali di persone morte con il morbo di Alzheimer hanno due tipi distinti di accumuli di proteine anormali: grovigli all’interno delle cellule e placche tra le cellule.
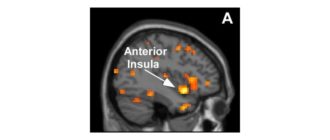
Questi segni distintivi dell’Alzheimer sono stati trovati principalmente nell’ippocampo, nella neocorteccia e in altre parti del cervello che si trovano sotto la corteccia e sono importanti per il pensiero, la memoria e l’apprendimento.
Tuttavia, come la ricerca ha sondato più profondamente nella malattia e le sue possibili cause, sono emersi problemi con la teoria dell’amiloide, affermano gli autori del nuovo studio.
Un problema riguarda le incongruenze nelle prove. Ad esempio, alcuni studi hanno riportato che, nonostante la presenza massiccia di placche di amiloide nel loro cervello, alcuni pazienti più anziani non mostravano deficit misurabili nel pensiero e nella memoria, mentre altri pazienti con sintomi di Alzheimer grave hanno mostrato una scarsa formazione di anormale proteina amiloide.
Un altro motivo per mettere in discussione la teoria dell’amiloide è che i farmaci sperimentali che hanno come bersaglio l’amiloide come un modo per curare l’Alzheimer hanno mostrato risultati deludenti negli studi clinici e non sono riusciti a fermare il declino.
Queste domande e questi problemi hanno portato i ricercatori a sostenere che placche e grovigli probabilmente emergeranno negli stadi successivi dell’Alzheimer e che sono coinvolti altri fattori scatenanti.
Un ruolo per i mitocondri?
I mitocondri sono piccoli compartimenti all’interno delle cellule in cui l’ossigeno e i nutrienti si trasformano in adenosina trifosfato (ATP), che è la principale fonte di combustibile per l’attività cellulare.
«Decenni di ricerca» hanno rivelato che questi powerhouse cellulari differiscono tra il cervello di Alzheimer e il cervello sano.
Ciò ha portato all’idea che i mitocondri svolgano un ruolo importante nell’Alzheimer, non solo come contributori ma anche come fattori guida della malattia.
L’attuale dibattito spazia dal suggerire che la beta amiloide causa la disfunzione mitocondriale nel proporre che una «cascata» di cambiamenti mitocondriali «sostituisca gerarchicamente» lo sviluppo della beta amiloide.
Un altro argomento nel dibattito propone che, nella malattia di Alzheimer, una forma «altamente tossica» di beta amiloide – nota come beta amiloide oligomerico – acceleri il declino mitocondriale che si verifica naturalmente con l’età.
Il nuovo studio, che esamina l’impatto della beta amiloide oligomerica sui mitocondri nelle cellule cerebrali, fornisce nuove prove in questa direzione.
Evidenza di rottura dei mitocondri
Per il loro studio, il dottor Mastroeni e colleghi hanno estratto i neuroni piramidali dall’ippocampo nel cervello di pazienti deceduti per il morbo di Alzheimer.
I neuroni piramidali sono stati descritti come i «motori e agitatori» del cervello e sono importanti per l’elaborazione cognitiva. Malattie degeneranti del cervello come l’Alzheimer sono note per uccidere in modo sproporzionato queste cellule.
Quando hanno studiato i neuroni piramidali dell’ippocampo, i ricercatori hanno trovato prove – sotto forma di ridotta espressione di molti geni mitocondriali – per suggerire che i loro mitocondri erano stati interrotti da beta amiloide oligomerico.
Hanno trovato la stessa espressione ridotta dei geni mitocondriali quando hanno esposto le cellule da una linea cellulare di neuroblastoma umano alla proteina tossica.
Altri tipi di cellule – come le cellule astrocitarie e microgliali – estratte dall’ippocampo dello stesso cervello affetto da malattia di Alzheimer, non hanno mostrato evidenze di mitocondri compromessi. Le cellule di astrociti e microglia forniscono supporto come il mantenimento dell’equilibrio chimico e la fornitura di nutrienti.
Il pre-trattamento può proteggere i neuroni
In un’altra serie di esperimenti, i ricercatori hanno pretrattato i neuroni umani in laboratorio con un composto che è strutturalmente simile al CoQ10, che è noto per aumentare l’ATP e limitare lo stress ossidativo, un altro processo che può degradare i mitocondri.
Quando hanno esposto i neuroni pretrattati alla beta amiloide oligomerica, hanno mostrato segni ridotti di deterioramento mitocondriale. Suggeriscono che questo risultato potrebbe aprire la strada a nuovi trattamenti per la malattia di Alzheimer.
«Questo studio rafforza la tossicità del beta amiloide oligomerico sui mitocondri neuronali e sottolinea l’importanza di composti protettivi per proteggere i mitocondri dalla tossicità dell’amiloide beta oligomerica».
Dr. Diego Mastroeni
Prospettive Future sulla Ricerca dei Mitocondri
Negli ultimi anni, la ricerca sui mitocondri ha acquisito slancio, rivelando il loro ruolo cruciale non solo nella produzione di energia, ma anche nella regolazione della morte cellulare e nella risposta infiammatoria. Studi recenti hanno dimostrato che interventi mirati a migliorare la funzione mitocondriale possono non solo proteggere i neuroni, ma anche promuovere la neurogenesi, la formazione di nuovi neuroni, in modelli preclinici di Alzheimer.
Alcuni ricercatori stanno esplorando l’uso di integratori nutrizionali, come l’acido alfa-lipoico e il resveratrolo, che mostrano promesse nel migliorare la salute mitocondriale. Inoltre, l’uso di terapie geniche potrebbe rappresentare una strategia innovativa per ripristinare la funzione mitocondriale nelle cellule cerebrali danneggiate.
La comprensione delle dinamiche mitocondriali nell’Alzheimer potrebbe aprire nuove strade per approcci terapeutici, puntando a preservare non solo la funzione cerebrale, ma anche la qualità della vita dei pazienti. Con il progresso delle tecnologie di imaging e delle piattaforme di screening ad alta capacità, il futuro della ricerca sui mitocondri nell’Alzheimer appare promettente.