Possiamo portare fino a 2 kg di microbi nel nostro intestino. All’interno delle decine di migliaia di miliardi di microrganismi che vivono ci sono almeno 1.000 specie di batteri costituiti da oltre 3 milioni di geni. Inoltre, due terzi del microbioma intestinale – la popolazione di microbi nell’intestino – è unico per ciascun individuo. Ma sai come il tuo microbiota intestinale potrebbe influenzare la tua salute?
Molti di noi sono consapevoli del fatto che i batteri nel nostro intestino svolgono un ruolo importante nella digestione. Quando lo stomaco e l’intestino tenue non sono in grado di digerire certi cibi che mangiamo, i microbi intestinali intervengono per offrire supporto, assicurandoci di ottenere i nutrienti di cui abbiamo bisogno.
Inoltre, i batteri dell’intestino sono noti per aiutare nella produzione di alcune vitamine – come le vitamine B e K – e svolgono un ruolo cruciale nella funzione immunitaria.
Tuttavia, sempre di più, i ricercatori stanno lavorando per scoprire di più su come i batteri intestinali – in particolare quelli unici per ciascuno di noi – influenzano la nostra salute e il rischio di malattia.
Uno degli aspetti più studiati è come il microbiota intestinale influisca sul rischio di obesità e altre condizioni metaboliche. Nel novembre 2014, ad esempio, è stato riportato uno studio che afferma che il nostro corredo genetico modella il tipo di batteri presenti nel nostro intestino, influenzando così il nostro peso.
In questo articolo, esploreremo il legame tra microbioma intestinale e obesità, oltre ad altre condizioni di salute potenzialmente sorprendenti.
Lo sviluppo del microbiota intestinale
Per lungo tempo, si è ritenuto che lo sviluppo del microbiota intestinale non iniziasse fino alla nascita, con il tratto gastrointestinale di un feto considerato un ambiente sterile.
Secondo Gut Microbiota Worldwatch – un servizio di informazione creato dalla European Society for Neurogastroenterology & Motility – il tratto digestivo di un neonato viene rapidamente colonizzato da microrganismi provenienti dalla madre e dall’ambiente circostante.
Il microbiota intestinale del bambino, per esempio, può essere influenzato dall’allattamento al seno. Gut Microbiota Worldwatch spiega che l’intestino dei bambini allattati al seno è principalmente popolato da batteri considerati «amici», a beneficio dell’intestino, mentre i bambini alimentati con formula tendono ad avere una diversità batterica inferiore.
Tuttavia, alcuni studi hanno messo in discussione l’idea che il feto sia un ambiente sterile, suggerendo che lo sviluppo del microbiota intestinale inizi prima della nascita.
Uno studio del 2008 ha identificato batteri nelle prime feci di topolini, noti come meconio, suggerendo che i batteri vengono trasferiti al feto dall’intestino della madre durante la gravidanza.
I ricercatori hanno inoculato un gruppo di topi gravide con batteri isolati dal latte materno umano e hanno scoperto batteri nel loro meconio, mentre non è stata trovata traccia di batteri nel gruppo di controllo.
«Sulla base della somma delle prove, è il momento di ribaltare il paradigma dell’utero sterile e riconoscere che il bambino non nato è stato colonizzato nel grembo materno», ha dichiarato Seth Bordenstein, biologo della Vanderbilt University di Nashville, TN.
Più diversità, migliore salute
Mentre il dibattito sul fatto che i bambini nascano con batteri intestinali continua, gli scienziati concordano su un punto: dalla nascita fino alla vecchiaia, il nostro microbiota intestinale è in continua evoluzione.
Come accennato in precedenza, due terzi del microbioma intestinale è unico per ciascuna persona, e questo è influenzato da ciò che mangiamo, dall’aria che respiriamo e da altri fattori ambientali. Alcuni studi hanno persino suggerito che la composizione del microbioma intestinale possa essere influenzata dai geni.
Ma come influisce questo microbiota unico sulla nostra salute? Questa è una domanda a cui i ricercatori sono sempre più interessati a rispondere.
Ricerche precedenti hanno suggerito che una maggiore varietà di batteri nell’intestino è associata a una migliore salute. Un recente studio ha scoperto che i neonati con una diversità batterica intestinale ridotta all’età di 3 mesi avevano maggiori probabilità di sviluppare allergie alimentari entro l’anno, suggerendo che la mancanza di diversità batterica nella prima infanzia potrebbe essere un fattore di rischio per le allergie.
Tuttavia, le implicazioni di un microbioma a bassa diversità non si fermano qui. Potresti rimanere sorpreso di apprendere come la mancanza o la sovrappopolazione di specifici batteri possa influire sulla tua salute.
Obesità
Studi recenti stanno esaminando l’associazione tra microbioma intestinale e aumento di peso, con alcuni scienziati che suggeriscono che la composizione dei batteri nell’intestino possa influenzare la suscettibilità individuale all’aumento di peso.
Nell’articolo precedente, abbiamo menzionato uno studio del 2014 in cui si affermava che i nostri geni potrebbero determinare quali batteri vivono nel nostro intestino e che questi batteri potrebbero influenzare il nostro peso corporeo.

In dettaglio, lo studio condotto da ricercatori della Cornell University e del King’s College London ha rilevato un ceppo di batteri più comune nelle persone con un peso corporeo sano, e la presenza di questo ceppo è altamente influenzata dai geni.
Inoltre, l’introduzione di questo batterio nel sistema dei topi ha portato a un guadagno di peso ridotto, suggerendo che questi batteri possano avere un effetto protettivo contro l’obesità.
«I nostri risultati mostrano che specifici gruppi di microbi intestinali potrebbero proteggere dall’obesità e che la loro abbondanza è influenzata dai nostri geni», ha affermato il prof. Tim Spector del King’s College di Londra. «Il microbioma umano rappresenta un nuovo ed entusiasmante target per modifiche dietetiche e terapie contro l’obesità».
Nel 2012, un altro studio suggeriva che la mancanza di batteri nell’intestino crasso potrebbe contribuire all’obesità rallentando l’attività del grasso bruno, che protegge dall’aumento di peso quando stimolato a bruciare calorie e grasso bianco.
Un caso clinico più recente ha rivelato come una donna che ha ricevuto un trapianto di microbiota fecale da un donatore in sovrappeso sia rapidamente diventata obesa dopo la procedura.
Sebbene la ricerca sia ancora in corso, è chiaro che i batteri intestinali meritano ulteriori indagini nel contesto dell’obesità.
Cancro
Negli ultimi anni, la connessione tra batteri intestinali e cancro ha attirato sempre più l’attenzione degli scienziati.
In uno studio del 2013, ricercatori statunitensi hanno scoperto batteri specifici nell’intestino che potrebbero essere correlati allo sviluppo del linfoma, un tipo di tumore dei globuli bianchi.
Un altro studio condotto da ricercatori britannici ha identificato un comune batterio intestinale che può causare cancro allo stomaco e ulcere duodenali disattivando parti del sistema immunitario coinvolte nella regolazione dell’infiammazione.
Nel 2014, è stata riportata una ricerca associando una specifica combinazione di batteri intestinali allo sviluppo del cancro del colon-retto. In questo studio, gli scienziati hanno somministrato antibiotici a topi con mutazioni genetiche note per causare polipi colorettali, scoprendo che questi topi non sviluppavano polipi, suggerendo un ruolo protettivo dei microbi intestinali.
Inoltre, i batteri intestinali sono stati trovati cruciali anche per migliorare l’efficacia dei trattamenti contro il cancro. Nel 2013, uno studio del National Cancer Institute ha dimostrato che l’immunoterapia e la chemioterapia erano meno efficaci in topi privi di batteri intestinali, mentre funzionavano molto meglio in topi con un microbioma intestinale sano.
Risultati simili sono stati registrati in un altro studio condotto da ricercatori francesi, dove un farmaco antitumorale risultava meno efficace nei topi con batteri intestinali limitati rispetto a quelli con una flora intestinale normale.
«Entrambi gli studi sono molto promettenti poiché mostrano collegamenti iniziali tra microbiota intestinale e risposta ai trattamenti», ha dichiarato Peter Turnbaugh dell’Università di Harvard. «Queste ricerche sottolineano l’importanza dei microbi nel determinare non solo la nostra predisposizione alla malattia, ma anche il nostro recupero da essa».
Salute mentale
Non molti di noi pensano a come i batteri intestinali possano influenzare il nostro stato mentale, ma in realtà giocano un ruolo fondamentale.
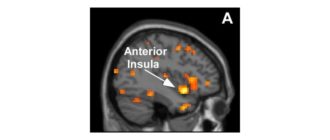
Secondo l’American Psychological Association (APA), i batteri intestinali producono una varietà di sostanze neurochimiche che il cervello utilizza per regolare processi fisiologici e mentali, come memoria, apprendimento e umore. Infatti, secondo l’APA, il 95% della serotonina del nostro corpo è prodotto dai batteri intestinali.

Con questo in mente, non sorprende che i batteri intestinali siano stati collegati a vari problemi di salute mentale, tra cui disturbi d’ansia e depressione.
Nel 2014, uno studio ha mostrato che i prebiotici – carboidrati che alimentano i batteri sani nell’intestino – possono ridurre lo stress e l’ansia. In questo studio, 45 adulti sani sono stati randomizzati a ricevere un prebiotico o un placebo quotidianamente per 3 settimane. Alla fine, i partecipanti che avevano assunto il prebiotico mostravano una minore attenzione agli stimoli negativi rispetto a quelli che avevano ricevuto il placebo, suggerendo una diminuzione dell’ansia in situazioni stressanti.
«Spesso sentiamo da pazienti che non si sono mai sentiti depressi o ansiosi fino a quando non hanno iniziato a riscontrare problemi intestinali», ha dichiarato il Dr. Kirsten Tillisch, autore principale dello studio. «Il nostro studio dimostra che la connessione tra intestino e cervello è una strada a doppio senso.»
Autismo
Si stima che l’autismo colpisca 1 bambino su 68 negli Stati Uniti. Mentre studi hanno associato fattori ambientali e genetici come potenziali cause del disturbo, i ricercatori stanno esaminando sempre più il ruolo dei batteri intestinali nel suo sviluppo.
Nel 2013, uno studio condotto dall’Arizona State University ha dimostrato che i bambini con autismo avevano livelli inferiori di tre tipi di batteri intestinali rispetto ai coetanei senza la condizione.
Uno studio più recente ha rivelato che le concentrazioni di metaboliti prodotti dai batteri intestinali nei campioni fecali dei bambini autistici differivano da quelle dei bambini senza il disturbo. Questo ha spinto i ricercatori a ipotizzare che i microbi intestinali possano alterare i metaboliti associati alla comunicazione tra intestino e cervello, interferendo così con la funzione cerebrale.
Un ulteriore studio ha dimostrato che un particolare batterio riduceva i sintomi autistici nei topi, rafforzando ulteriormente l’associazione tra microbiota intestinale e autismo.
Possiamo modificare i nostri batteri intestinali?
Poiché il microbioma intestinale è influenzato dal cibo che mangiamo e dall’ambiente circostante, è logico pensare che esistano modi per renderlo più sano.
Secondo la Mayo Clinic, una dieta equilibrata può favorire la presenza di batteri intestinali benefici. Il consumo di cibi fermentati – come il miso e i crauti – è stato dimostrato aumentare i livelli di batteri fermentanti nell’intestino. Inoltre, frutta e verdura contengono fibre e zuccheri che possono migliorare la salute del microbiota intestinale.
L’esercizio fisico è un altro aspetto chiave per migliorare la diversità del microbiota intestinale. Uno studio pubblicato nel giugno 2014 ha confrontato i batteri intestinali di 40 giocatori di rugby professionisti con quelli di due gruppi di controllo, rivelando che i giocatori presentavano livelli significativamente più alti di un batterio associato a un ridotto rischio di obesità.
In un editoriale collegato, il Dr. Georgina Hold dell’Università di Aberdeen ha sottolineato l’importanza di comprendere come migliorare la salute attraverso la modulazione del microbiota intestinale: «Con l’aumento dell’aspettativa di vita, è fondamentale capire come mantenere una buona salute. Non è mai stato più rilevante rispetto al nostro microbiota. Sviluppare nuove modalità per sfruttare le proprietà benefiche del nostro microbiota, integrando le pratiche salutari nella vita moderna, dovrebbe essere un obiettivo primario.»